
UT 西南大学的研究人员报告了第一个结构确认,即内源性或自制分子可以通过称为 TLR4-MD-2 受体复合物的一对免疫细胞蛋白引发哺乳动物的先天免疫。这项工作对于寻找治疗和可能预防自身免疫性疾病(如多发性硬化症和抗磷脂综合征)的方法具有广泛的意义。
TLR4-MD-2 受体复合物因其在人体对革兰氏阴性菌感染的反应中的作用而闻名。长期以来,人们一直怀疑它在自身免疫中的作用,尽管缺乏直接证据。该团队由诺贝尔奖获得者、宿主防御遗传学中心 (CGHD) 主任、医学博士 Bruce Beutler 领导,确定了称为硫苷脂的脂质,可以激活位于细胞膜上的先天免疫传感器 TLR4。他发现了 TLR4 受体背后的基因及其在人体对感染的最早反应(先天免疫)中的作用,这使他获得了 2011 年的诺贝尔生理学或医学奖。
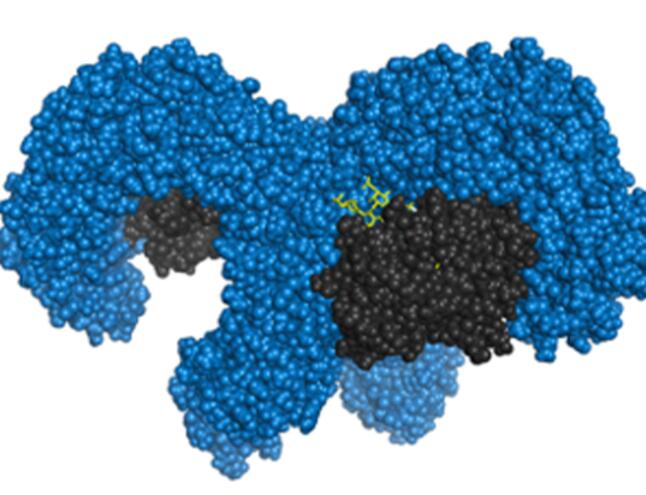
Beutler 是本周发表在《美国国家科学院院刊》上的研究的通讯作者,该研究使用 X 射线晶体学来确认硫苷脂如何与受体复合物结合。主要作者 Lijing Su 博士是 CGHD 助理教授,在生物物理学方面具有二级任命,在 UT Southwestern 的结构生物学核心设施和伊利诺伊州的阿贡国家实验室进行了 X 射线晶体学研究。
“多年来,内源性或自身分子是否可以激活先天免疫受体的问题一直是一个重要的问题,”免疫学和内科学教授 Beutler 说。“科学家们观察到我们自己的核酸可以激活 TLR 3、7、8 和 9,从而引起炎症和自身免疫。已经提出了许多 TLR4 的内源性配体,其中大部分是蛋白质。这是第一个证实存在的研究通过结构研究,这种 TLR4 配体意味着一种适合受体的分子。”
该团队对小鼠 TLR4-MD-2 与硫苷脂复合物的结构研究,详细了解了硫苷脂如何与受体复合物的 U 形侧结合以激活它。这种结合引发了导致身体炎症反应的生物途径。
这项研究提出了新的重要问题,包括一些关于受体在小鼠和人类中反应方式差异的观察结果。它还提出了关于单个硫苷脂的化学组成如何影响它们与受体复合物相互作用以激活或抑制免疫反应的方式的新问题。
“我们的工作表明,这些或其他内源性脂质可能确实会触发 TLR4 的激活,”Beutler 说,并补充说 TLR4 通常充当脂多糖(一种脂质加糖分子)——也称为内毒素——的传感器。驻留在革兰氏阴性菌上。TLR4-LPS 结合与败血症有关,败血症是一种潜在的致命疾病,在这种情况下,免疫系统因感染而进入超速运转状态。
Su 补充说,她和 Beutler 实验室的其他人之前报告说,TLR4 及其共同受体 MD-2 可以被一种名为 Neoseptin-3 的合成小分子激活,该分子与 Dale Boger 博士的实验室合作创建,在斯克里普斯研究所,该研究所与天然微生物配体 LPS 没有结构相似性。
“我们的小鼠 TLR4-MD-2 与 Neoseptin-3 复合物的晶体结构表明,这种受体复合物可能容纳多个小分子,而不是像 LPS 这样的大分子,”Su 解释说。“这一结果促使我们寻找可能结合和激活 TLR4-MD-2 信号传导的天然脂质。早期候选物包括磷酸神经酰胺,但这些未能激活受体。硫苷脂的结构特征以及它们在某些组织中的丰度,导致我们改为测试它们,我们证实一些硫苷脂确实激活了 TLR4。”
UTSW 的合著者包括 Ying Wang、Tao Yao、Jianhui Wang 和 Eva Marie Y. Moresco。来自以色列、匹兹堡、宾夕法尼亚和德国的研究人员也参与了这项工作。
该调查得到了美国国立卫生研究院(资助 AI125581 和 AI100627)、Lyda Hill 基金会、以色列癌症协会(资助 20180115)、以色列科学基金会(资助 2142/20)和以色列科学部的支持。阿贡的工作得到了美国能源部的支持(合同 DE-AC02-06CH11357)。该研究还得到了 NIH 主任办公室的支持(奖项 S10OD025018)。
Beutler 是一位摄政教授,担任 Raymond 和 Ellen Willie 癌症研究杰出主席,以纪念 Laverne 和 Raymond Willie, Sr.